XBridge Premier色譜柱助力SEC-MALS系統在生物藥品表征分析中的應用

SEC-MALS技術廣泛應用于生物制藥領域,是一種不可或缺的、關鍵性的、高效且可靠的分析表征手段。其中經典配置為Waters Arc Premier HPLC與懷雅特(Wyatt)多角度激光光散射儀DAWN?、干涉型示差折光檢測器Optilab?(dn/dc儀)聯用,在此基礎上再搭配使用XBridge? Premier系列尺寸排阻色譜柱,可以顯著增強其系統性能,拓展其在生物醫藥領域的應用場景。本應用文獻將介紹配備了XBridge Premier Protein、XBridge Premier GTx BEH SEC色譜柱的SEC-MALS系統,如何分析表征治療性單抗mAbs、生物相似藥和腺相關病毒粒子AAVs等多個關鍵質量屬性。
SEC-MALS(由體積排阻分離色譜SEC、多角度激光光散射儀DAWN、紫外檢測器UV和干涉型示差折光檢測器Optilab聯用組成)作為一種簡單、穩健的方法早已被廣泛用于定性和定量蛋白和其它生物制藥的各種關鍵質量屬性,例如,絕對摩爾質量Mw、聚集體、純度、偶聯物、空包率及有效載荷等屬性。SEC-MALS系統是一種無需試劑處理樣品、可實現自動化且符合QA/QC實驗室要求的標準分析工具。
成功的SEC-MALS分析方法開發的第一步需要摸索良好的色譜條件,但選擇合適的色譜柱以及優化色譜條件可能需要耗費很長時間。XBridge Premier作為SEC平臺分析方法色譜柱,可節省大量方法開發時間。與MALS聯用定量蛋白和AAVs多質量屬性方面,比傳統硅基填料色譜柱具有更好的耐用性和更高的靈敏度。
材料與方法
儀器
SEC體積排阻色譜系統:
Waters Arc Premier HPLC系統,其中包括2998 PDA UV檢測器(可同時采集280 nm、260 nm)
18角度激光光散射儀MALS:
DAWN,內置在線動態激光光散射模塊Wyatt QELS
干涉型示差折光檢測器dRI(dn/dc儀):
Optilab
光散射數據分析處理軟件:
ASTRA? software

圖1. SEC-MALS系統:HPLC模塊(泵、自動進樣器和PDA)、18角度激光光散射儀DANW和干涉型示差折光檢測器Optilab。
色譜柱
Waters XBridge Premier系列色譜柱有兩大技術優勢:一方面它具有Waters MaxPeak? Premier高性能表面(保護對金屬敏感的分析物)和2.5 μm BEH- PEO材質填料,與傳統5 μm硅基色譜柱相比,它更適合SEC-MALS系統。
蛋白質
色譜柱1:
XBridge Premier Protein SEC column,250 ?,7.8 mm x 300 mm
色譜柱2:
Wyatt Technology的硅基SEC柱,300 ?,7.8 mm x 300 mm
流動相:
Dulbecco’s PBS (10 mM Na2 HPO4, 1.8 mM KH2 PO4, 137 mM NaCl, 2.7 mM KCl, 3.1 mM NaN3? pH 6.7)
流速:
0.5 mL/min
樣品:
Herceptin (trastuzumab): 10 μL/21 mg/mL
Kanjinti (trastuzumab biosimilar): 10 μL/21 mg/mL
Pertactin: 50 μL at 0.5 mg/mL
UT antibody: 50 μL at 1.0 mg/mL
感謝由德克薩斯大學奧斯汀分校提供的Pertactin和UT antibody。
AVV
樣品:
empty和full AAV8樣品
色譜柱:
分別使用XBridge Premier GTx BEH SEC column 450 ?, 7.8 mm x 300 mm或者Wyatt Technology AAV column, 500 ?, 4.6 mm x 300 mm分離
流動相:
根據Wyatt’s AAV SOP Guidance Manual配制,流速設定0.5 mL/min,詳細分析方法詳見Wyatt的AAV SOP Guidance Manual(ASTRA軟件中Viral Vector Analysis Method)。
結果與討論
平臺色譜柱技術減少液相色譜方法開發
非理想色譜行為產生于樣品和色譜柱之間,由于非位阻相互作用而產生的次級相互作用,可能會導致相對于標準品洗脫時間的變化、色譜峰拖尾以及其他不利影響。這些液相色譜中的現象會導致傳統分析型SEC分析的不確定性,可能需要投入大量的時間和資源來優化方法從而改善色譜分離效果。如本文所述,只需使用XBridge Premier Protein SEC色譜柱替代通用硅基SEC色譜柱就可以顯著改善的分離效果。
Pertactin是Bordetella pertussis細菌的一種高度免疫原性的毒性因子,這種細菌引起百日咳,并可用于生產非細胞(組成)的百日咳疫苗。如(圖2上)所示,由于二次相互作用,Pertactin從常規的硅基色譜柱中洗脫時呈現出分裂峰。然而,在不改變流動相、流速或進樣量的情況下,Pertactin從XBridge色譜柱中洗脫時出現一個明確定義的單體峰(圖2下)。兩種情況下,MALS均提供了摩爾質量的絕對定量,另外MALS定量證實第二個峰不是由于色譜柱上二聚體解離或其它共同洗脫樣品而產生(圖2上)。

圖2. XBridge Premier色譜柱實現理想的色譜分離效果。Pertactin分別使用傳統的硅基SEC柱(圖2上)和XBridge Premier Protein SEC柱(圖2下)分離,通過MALS獲取色譜信號及確定摩爾質量。
SEC-MALS分析蛋白的技術優勢
盡管XBridge Premier 色譜柱得到了峰型良好的色譜峰和高分辨率,但是Pertactin單體(60KD)竟然比BSA單體(66KD)更先被洗脫出來。如圖3所示,這種反常現象是否與蛋白構象的差異有關? DAWN 的QELS組件提供的在線DLS測試有助于準確做出判斷。BSA單體流體力學半徑Rh測定值是3.5 nm,而Pertactin單體Rh測定值是4.0 nm (圖3所示)。Rh與洗脫順序的對應關系(尺寸越大,越先被洗脫)表明色譜條件合適,分子的分離是基于擴散尺寸也就是Rh的差異實現分離。值得注意的是,這兩種蛋白的尺寸差異與它們的分子量無對應關系,進一步凸顯了SEC-MALS測定絕對/真實分子量的重要意義。

圖3. BSA和Pertactin 流體力學半徑Rh(Wyatt QELS模塊測定)與光散射信號疊加圖。
傳統柱校正方法存在一定局限性,尤其當樣品與色譜柱存在相互作用的時候,這種局限性更加明顯。如圖4,SEC-MALS可以準確測定UT單抗單體,BSA單體以及BSA二聚體的分子量(圖4上),但是UT抗體單體相較于BSA二聚體洗脫順序異常。
在線 DLS 表明,與Pertactin有所不同,UT單抗的分離不僅僅是基于流體力學半徑Rh的差異。如(圖4下)所示,UT單抗單體的Rh(5.6 nm)要比的Rh(4.4 nm)大的多,但是UT單抗單體卻晚于BSA二聚體洗脫,可能的原因是UT單抗與色譜柱存在相互作用。優化色譜條件,減少相互作用對于很多樣品來說,需要耗費大量時間和精力。MALS不依賴洗脫時間,可直接測定分子量,同時在線DLS確認洗脫順序是否理想。因此SEC-MALS大大降低了色譜條件優化的難度,從而節約了時間和成本。

圖4. 無論洗脫次序如何,MALS都可以準確測定分子量。上圖是MALS測定的分子量與光散射信號的色譜疊加圖。下圖是在線DLS測定的流體力學半徑Rh與光散射信號的色譜疊加圖。
SEC-MALS評估生物藥相似性
證明生物類似藥與創新藥物具有生物相似性是抗體類藥物進入市場的一個壁壘。生物相似性研究涉及大量的體內試驗,推高了生物類似藥的研發成本和價格,使得一些患者無力承擔他們所需的救命藥。更好的體外生物相似性試驗可以減輕體內試驗的一些壓力,從而減少將生物類似抗體推向市場所需的時間、成本和資源。
以下試驗通過SEC- MALS分析和比較創新藥-曲妥珠單抗Herceptin和生物類似藥Kanjinti的相似性。如圖5(左)所示,Herceptin和Kanjinti的單體和二聚體的摩爾質量是相同的,分別為~160 kDa和~300 kDa。此外,兩種產品均含有98%的單體和~1%的二聚體。如圖5(右)所示,XBridge Premier色譜柱可以將樣品中的單體和低分子量(LMW)組分分離。兩種藥物均含~1% 低分子量組分;然而兩種藥物的低分子量組分的摩爾質量不同,Kanjinti 的為47 kDa, Herceptin 的為60 kDa。
有趣的是,光散射數據也揭示了兩種藥物的高分子量(HMW)組分的差異。由于光散射強度與濃度和摩爾質量成正比,因此MALS特別適合于檢測和定量蛋白質聚集體,對于低濃度的蛋白質聚集體在僅使用UV或RI作為檢測器時可能無法被檢測到。在這個案例中,Herceptin中含有一個特別的高分子量組分,這種高分子量組分在Kanjinti中不存在,這個高分子量組分的Rh為11 nm,Mw為1.4 MDa,僅占占總質量的0.1%,但可以通過MALS清晰識別。

圖5. MALS能夠對單克隆抗體的體外生物物理相似性進行詳細的比較。左圖為由MALS測定的LS色譜圖和分子量疊加圖。右圖為LS色譜圖的局部放大圖。
SEC-MALS系統中使用GTx gene therapy色譜柱增強AAV多種質量屬性定量分析(MAQTM)
AAV病毒是一種單鏈DNA病毒,已經成為一種常用的基因治療遞送載體。由SEC-MALS定量AAV關鍵質量屬性包括病毒滴度,實心率和聚體含量。SEC-MALS提供了一種穩健和易于操作的方法,該方法可以在低于30 min內檢測上述關鍵質量指標和額外的表征信息。
圖6顯示了用SEC-UV-MALS-RI分析的2批次AAV樣品。通過結合多角度光散射信號,dRI和280 nm以及260 nm的數據,可以測定洗脫峰所對應的蛋白衣殼及DNA的摩爾質量,并量化色譜圖中每個點的衣殼滴度和有效載荷。實心和空心AAVs都能從XBridge Premier GTx column很好地洗脫下來,并從二聚和更高的聚體中分離出來。如圖6所示,SEC-MALS法檢測了單體峰對應的衣殼和核酸摩爾質量。
除了可以定量衣殼和DNA的摩爾質量外,ASTRA軟件的Viral Vector分析方法可同時定量AAV物理滴度(Cp)和實心率(Vg/Cp),具體總結見表1。雖然兩個實心AAV樣品有相似的衣殼含量(Vg/Cp ~ 1),但樣品1實心的濃度只有樣品2的一半。

圖6.兩個實心AAV樣品的多種質量屬性定量分析結果與光散射信號。上圖,具有摩爾質量的LS信號。下圖為具有顆粒濃度與LS信號。
XBridge Premier GTx 色譜柱也能提供比傳統硅基填料色譜柱更靈敏的SEC-MALS結果。如圖7所示,洗脫下來的病毒滴度的測量值非常接近進樣的病毒滴度,甚至低于當前的LOQ,即5 x 10e+10 particles/mL(見ASTRA AAV SOP,該數值是由傳統的7.8 × 300 mm硅基色譜柱測定)。靈敏度的提升有助于節省寶貴的樣品或增加信噪比,同時增加了方法的穩健性。
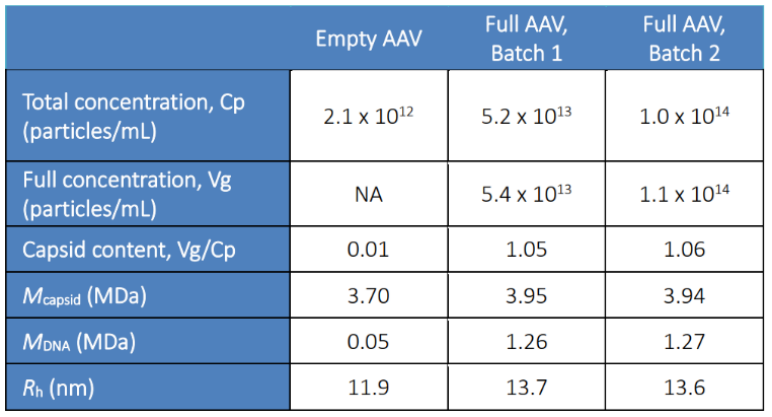
表1. 通過組合SEC-UV-MALS測得的多種關鍵質量參數,AAV8樣品由貝勒藥學院提供。

圖7. 用7.8 x 300 mm XBridge Premier GTx色譜柱測得的定量限低于傳統的同尺寸硅基色譜柱測得的定量限。
量化較大尺寸的AAV聚集物
如圖8所示,硅膠材質的4.6 mm SEC色譜柱只能部分分離AAV聚合物和單體。相比之下,7.8 mm GTx SEC色譜柱可將聚合物完全分離出主單體峰,甚至提供了不同聚合物亞種的分辨率。這種聚合物分辨率的提高有助于更好地識別和定量分析聚合物和顆粒污染,因此在AAV質量控制中非常有用。
然而,SEC可能會破壞或以其它方式過濾高聚體。對更高程度的聚集體種類進行更加準確的定量分析需采用FFF-MALS(非對稱型場流分離檢測系統)。由于沒有固定相,不會剪切或過濾掉高聚物,FFF-MALS可作為尺寸排阻分離法補充或交叉驗證手段。
此外,已經發現通過UV或熒光對高聚體進行定量分析往往會大大高估它們的豐度,但MALS信號可提供更準確的定量分析。

圖8.聚集體的放大色譜圖。比較中使用的是貝勒醫學院提供的AAV8血清型第1批次的實心AAV樣品。WTC AAV色譜柱是4.6 mm x 300 mm的硅基柱。XBridge Premier GTx是7.8 mm x 300 mm的色譜柱。
結 論
使用XBridge Premier 色譜柱作為SEC通用平臺分析柱,能提供更優異的分離能力和高質量的光散射數據。對于蛋白,XBridge Premier色譜柱能夠提供優異的分離度并能顯著降低蛋白和色譜柱間的相互作用力,而幾乎不需要額外方法優化,適用于治療類抗體到疫苗抗原等多種分析樣本。利用MALS和高分辨率色譜還能實現體外生物類似物的分析,生物藥生產企業能快速鑒定有用的趨勢和關鍵質量屬性,進而節省后續的體內試驗的時間和資源。
對于AAV方面的應用,XBridge Premier GTx色譜柱能保證高靈敏度、高回收率和理想的光散射數據質量,有助于成功實現AAV樣品的多質量屬性分析。使用傳統技術,這些關鍵質量屬性需要多種復雜的儀器,例如ELISA用來檢測物理滴度,qPCR用來檢測基因滴度,或AUC用來檢測空實率。但SEC-MALS一次進樣就可以同時測量這些關鍵質量屬性。
總之,由于XBridge Premier Protein SEC色譜柱和XBridge Premier GTx色譜柱優異的色譜性能,結合Wyatt MALS,為表征治療性蛋白藥物和AAV藥物提供了理想的解決方案。高性能SEC色譜柱意味著MALS能夠更精細和更可靠的定量多質量屬性。
致 謝
感謝德克薩斯大學奧斯汀分校提供的Pertactin和UT抗體樣品,感謝貝勒醫學院提供的實心和空心AAV樣品。
引用文獻
1. Liu, J., Eris, T., Li, C., Cao, S . & Kuhns, S . Assessing Analytical Similarity of Proposed Amgen Biosimilar ABP 501 to Adalimumab. BioDrugs 30, 321–338 (2016).
2. Troxell, B. et al. Application of Size Exclusion Chromatog- raphy with Multiangle Light Scattering in the Analytical Development of a Preclinical Stage Gene Therapy Program . Hum Gene Ther 34, 325–338 (2023).
3. Fu, Y. et al. Comprehensive biophysical characterization of? ?AAV-AAVR interaction uncovers serotype- and pH-depend- ent interaction. Journal of Pharmaceutical and Biomedical Analysis 234, 115562 (2023).
4. Bartalis, J et al.AN2004: Why and how to quantify AAV ag- gregates by FFF-MALS.
5. Bian, J., Gobalasingham, N ., Purchel, A. & Lin, J. The Power of Field- Flow Fractionation in Characterization of Nano-? particles in Drug Delivery. Molecules 28, 4169 (2023) .





































